¿La temperatura afecta la disolución?
Video de resumen de la leccion para maestros
Nota: Este video está diseñado para ayudar al maestro a comprender mejor la lección y NO está destinado a ser mostrado a los estudiantes. Incluye observaciones y conclusiones que los estudiantes deben hacer por sí solos.
Los subtítulos están disponibles en inglés y español para todos los videos.
Conceptos clave
- Al añadir energía (calentar) aumenta el movimiento molecular.
- El aumento del movimiento molecular compite con la atracción entre las moléculas de soluto, tendiendo a hacer que se separen con más facilidad.
- El aumento del movimiento molecular provoca que más moléculas de disolvente entren en contacto con moléculas de soluto y las atraigan con más fuerza, lo que normalmente provoca una mayor disolución.
- Dado que las diferentes sustancias están hechas de diferentes átomos, iones o moléculas, el aumento de la temperatura afectará su disolución en diferentes grados.
Resumen
Los alumnos vuelven a repasar la actividad de disolución de los M&M de la Lección 4. Diseñarán un experimento para ver si la temperatura afecta cuánto se disuelve el recubrimiento de azúcar de un M&M.
Objetivo
Los alumnos podrán identificar y controlar las variables para diseñar un experimento y ver si la temperatura de un disolvente afecta la velocidad a la que se disuelve un soluto. Los alumnos podrán explicar, a nivel molecular, por qué el aumento de la temperatura aumenta la tasa de disolución.

Seguridad
Ten cuidado al manipular el agua caliente.
Materiales para cada grupo
- M&M (3 del mismo color)
- 3 vasos de plástico transparente
- 1 hoja de papel blanco
- Agua a temperatura ambiente
- Agua caliente (aproximadamente a 50 °C)
- Agua fría (a unos 5 °C)
Materiales para la demostración
- 4 cilindros graduados (50 ml)
- Agua caliente (aproximadamente a 50 °C)
- Agua fría (a unos 5 °C)
- Sal
- Azúcar
- Cuchara
- 2 vasos pequeños
Descarga todos los recursos de la Lección 5.6
Obtenga el plan de lección completo y la hoja de actividades para la "Lección 5.6: ¿La temperatura afecta la disolución?"
Instrucciones
1 Involúcrate
Paso 1
Pide a los alumnos que trabajen en grupos para diseñar un experimento para investigar si la temperatura del agua afecta la cantidad de recubrimiento de los M&M que se disuelven.
Recuerda a los alumnos el experimento que hicieron en la Lección 4, en el que colocaron un M&M en agua y vieron disolverse el recubrimiento de azúcar de color. En ese experimento, los alumnos utilizaron agua y luego alcohol y aceite para ver si el disolvente utilizado afecta la disolución del recubrimiento de los M&M.
Pregunta a los alumnos:
- ¿Qué podrían investigar sobre cómo se disuelven los M&M en agua?
Si los alumnos no sugieren cambiar la temperatura del agua, pregunta si creen que la temperatura del agua afecta la cantidad de recubrimiento que se disuelve.
Pide a los alumnos que comenten, en grupos, las siguientes preguntas:
- ¿Cómo podrían investigar si la temperatura del agua afecta la cantidad de recubrimiento que se disuelve de un M&M?
- ¿Cuáles son las variables de este experimento y cómo las controlarán?
A medida que visitas los grupos y escuchas sus conversaciones, comprueba si los alumnos están pensando en variables como:
- Tipo de contenedor
- Cantidad de agua
- Color de los M&M
- Cuándo los M&M se colocan en el agua
- Ubicación de los M&M en cada vaso
Todas estas variables deben mantenerse iguales. Los alumnos deben darse cuenta de que la única variable que se debe cambiar es la temperatura del agua.
Paso 2
Pide a los grupos de alumnos que compartan sus ideas para comparar el efecto de la temperatura en la disolución y considera cómo cada plan controla las variables.
A medida que cada grupo presenta sus planes, pide a la clase que identifique cómo cada plan controla las variables. Algunos grupos pueden haber planeado probar colocar los M&M en agua caliente y fría, pero no tuvieron en cuenta el uso de agua a temperatura ambiente. Anima a todos los grupos a que hagan pruebas con los M&M en las tres temperaturas del agua. El agua a temperatura ambiente sirve de control y puede ayudar a los alumnos a ver la diferencia en cómo afecta la temperatura la disolución.
2 Evalúa
Entrega a cada alumno una hoja de actividades.
- Lección 5.6 Hoja de actividades PDF | DOCX | Google Doc
- Lección 5.6 Respuestas de la hoja de actividades PDF | DOCX | Google Doc
Descarga la hoja de actividades y distribuya una por alumno.
La hoja de actividades servirá como el componente de evaluación de cada plan de lección 5-E. Las hojas de actividades son evaluaciones formativas del progreso y la comprensión de los alumnos. Al final de cada capítulo se incluye una evaluación sumativa más formal.
Los alumnos describirán el diseño de su experimento, registrarán sus observaciones y responderán preguntas sobre la actividad en la hoja de actividades. Las secciones Explícalo con átomos y moléculas y Aprende más de la hoja de actividades se completarán en conjunto con la clase, en grupos o individualmente, según tus instrucciones. Observa la versión para el maestro de la hoja de actividades para encontrar las preguntas y respuestas.
3 Explora
Paso 3
Pide a los grupos que coloquen un M&M en agua fría, a temperatura ambiente y caliente al mismo tiempo para investigar el efecto de la temperatura en la disolución.
Pregunta para investigar
¿Afecta la temperatura del agua la cantidad de recubrimiento de un M&M que se disuelve?
Materiales para cada grupo
- 3 M&M del mismo color
- 3 vasos de plástico transparente
- 1 hoja de papel blanco
- Agua a temperatura ambiente
- Agua caliente (aproximadamente a 50 °C)
- Agua fría (a unos 5 °C)

Procedimiento
- Vierte agua fría, agua a temperatura ambiente y agua caliente en los vasos de modo tener suficiente agua como para cubrir un M&M.
- Coloca los tres vasos sobre el papel blanco. Escribe “Frío”, “Temperatura ambiente” y “Caliente” cerca del vaso correspondiente.
- Con la ayuda de tus compañeros, coloca un M&M del mismo color en el centro de cada vaso al mismo tiempo. Observa durante aproximadamente 1 minuto.
Resultados esperados
Más colorante y azúcar se disuelven del M&M que está en el agua caliente, y en menor medida en el agua fría y a temperatura ambiente. Esto significa que hay más chocolate visible en el M&M que está en agua caliente que el que está en el agua fría y a temperatura ambiente. El colorante y el azúcar en el agua a temperatura ambiente se disuelven en algún punto intermedio entre el agua fría y el agua caliente, pero de manera más similar al agua fría que a la caliente.
Nota: En realidad, en esta actividad hay dos procesos. El colorante y el azúcar se disuelven en el agua, pero también se disipan en el agua. La temperatura del agua afecta la cantidad que se disuelve, pero también afecta la velocidad de disipación. Los alumnos deben centrarse en la superficie del M&M para analizar la cantidad de colorante y azúcar que se disuelve.
Paso 4
Registra y comenta las observaciones de los alumnos.
Pregunta a los alumnos:
- ¿Afecta la temperatura del agua la cantidad de recubrimiento con color de un M&M que se disuelve? ¿Cómo lo sabes?
En base a tus observaciones, los alumnos deben concluir que el agua más caliente provoca una mayor disolución. Es posible que los alumnos hayan notado una mayor diferencia en la cantidad que se disuelve entre el agua caliente y el agua a temperatura ambiente que entre el agua a temperatura ambiente y el agua fría. Si no hay comentarios al respecto, sugiere que hay una diferencia.
4 Explica
Paso 5
Comenta cómo las diferencias en el movimiento molecular causaron que más cantidad del recubrimiento de azúcar se disuelva en agua caliente que en agua fría.
Pregunta a los alumnos:
- ¿Cuáles son las diferencias en la forma en que las moléculas de agua se mueven en agua fría, agua a temperatura ambiente y agua caliente?
Los alumnos deben recordar que las moléculas de agua se mueven más rápido en agua caliente que en agua fría. - ¿Por qué crees que el azúcar se disuelve mejor en agua caliente que en agua fría?
El motivo por el que el azúcar se disuelve a una mayor velocidad en el agua caliente tiene que ver con un mayor movimiento molecular. La energía añadida al agua caliente hace que las moléculas de agua se muevan más rápido y las moléculas de sacarosa vibren más rápido. Este movimiento añadido tiende a hacer más fácil superar los enlaces entre las moléculas de sacarosa. Cuando las moléculas de agua de movimiento más rápido se unen a las moléculas de sacarosa, una mayor proporción de estas interacciones sacarosa-agua tienen suficiente energía para alejar las moléculas de sacarosa de otras moléculas de sacarosa, por lo que aumenta la tasa de disolución. - Por qué piensas que hay una mayor diferencia en la cantidad que se disuelve entre el agua caliente y el agua a temperatura ambiente que entre el agua a temperatura ambiente y el agua fría?
Existe una mayor diferencia en la tasa de disolución porque existe una mayor diferencia en la temperatura entre el agua caliente y a temperatura ambiente (unos 30 grados) que entre el agua a temperatura ambiente y el agua fría (unos 15 grados).
5 Explora
Paso 6
Realiza una demostración o muestra un video para investigar si todas las sustancias se disuelven mucho mejor en agua caliente que en agua fría.
Pide a los alumnos que hagan una predicción:
- En la actividad, han visto que el agua caliente disuelve el azúcar mejor que el agua fría. ¿Creen que la sal se disolverá mucho mejor en agua caliente que en agua fría, como el azúcar?
Proyecta la imagen Agua caliente y fría disuelven sal y azúcar.
Si decides realizar la demostración, sigue el procedimiento descrito a continuación.
Pregunta para investigar
¿La sal se disolverá mucho mejor en agua caliente que en agua fría, como el azúcar?
Materiales para la demostración
- 4 cilindros graduados (50 o 100 ml)
- Agua caliente (aproximadamente a 50 °C)
- Agua fría (a unos 5 °C)
- Sal
- Azúcar
- Cuchara
- 4 vasos pequeños
Preparación del maestro
- Etiqueta dos vasos pequeños de sal y dos vasos de azúcar.
- Coloca 1 cucharada de sal y 1 cucharada de azúcar en cada uno de los vasos etiquetados.
Procedimiento
Sal en agua fría y caliente
- Coloca 25 ml de agua caliente y 25 ml de agua fría en dos cilindros graduados separados.
- Al mismo tiempo, vierte una cucharada de sal en cada cilindro graduado. No los remuevas, agites ni revuelvas. Coloca estos cilindros graduados a un lado.

Azúcar en agua fría y caliente
- Coloca 25 ml de agua caliente y 25 ml de agua fría en dos cilindros graduados separados.
- Al mismo tiempo, vierte una cucharada de azúcar en cada cilindro graduado. No los remuevas, agites ni revuelvas. Coloca estos cilindros graduados a un lado.
Compara las cantidades de sal y azúcar que quedan sin disolver.
- Muestra a los alumnos los cilindros graduados con la sal.
- Muestra a los alumnos los cilindros graduados con el azúcar.
Resultados esperados
El azúcar es menos visible en el agua caliente que en el agua fría, lo que significa que más azúcar se disuelve en el agua caliente que en el agua fría. No hay ninguna diferencia evidente entre la cantidad de sal que se disuelve en el agua caliente y el agua fría. Esto muestra que la temperatura afecta la disolución del azúcar más que la disolución de la sal.
Paso 7
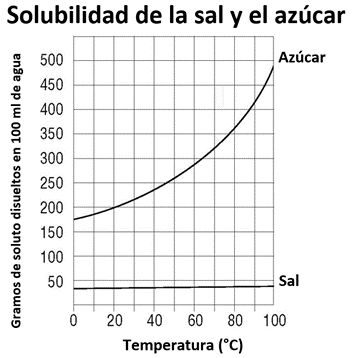
Muestra a los alumnos la tabla y el gráfico para ver la solubilidad del azúcar y la sal a diferentes temperaturas.
Proyecta el gráfico Solubilidad de la sal y el azúcar.
Ayuda a los alumnos a entender que el gráfico muestra que más azúcar se disuelve en agua a medida que aumenta la temperatura del agua. Ayúdales también a ver que la disolución de la sal también aumenta a medida que aumenta la temperatura del agua. Pero la disolución de la sal no aumenta tanto como la del azúcar.
| Comparación de la solubilidad del cloruro de sodio y la sacarosa Medido en gramos de soluto disueltos en 100 ml de agua | ||||||
| Temperatura °C | 0 | 20 | 40 | 60 | 80 | 100 |
| Cloruro de sodio | 35.5 | 36 | 36.5 | 37.5 | 38 | 39 |
| Sacarosa | 179 | 204 | 241 | 288 | 363 | 487 |
Nota: Los alumnos pueden preguntar por qué se disuelve mucho más el azúcar a temperaturas más altas en comparación con la sal. Esto no es fácil de explicar a nivel molecular para alumnos de la escuela media, la secundaria o aún de nivel universitario. Diles a los alumnos que, puesto que las sustancias están compuestas por átomos, iones y moléculas diferentes, se mantienen unidas de manera diferente e interactúan con el agua de manera diferente. El cambio de temperatura también afecta el movimiento de los átomos, iones o moléculas de la sustancia y afecta la interacción entre las moléculas de agua y las partículas de la sustancia. Hay tantos factores implicados que es difícil explicar por qué un aumento de la temperatura afecta más la solubilidad de una sustancia que la de otra.
Pregunta a los alumnos:
- La demostración mostró que la temperatura afecta más la disolución del azúcar que la disolución de la sal. Explica cómo el gráfico muestra esto. A medida que aumenta la temperatura, se puede disolver cada vez más azúcar, pero solo se puede disolver un poco más de sal.
- ¿Cuánta azúcar se disuelve en 100 ml de agua a 50°C? Se disolverán unos 260 g de azúcar.
- ¿Cuánta sal se disuelve en 100 ml de agua a 50 °C? Se disolverán unos 37 g de sal.
6 Amplía
Paso 8
Traza una curva de solubilidad para el cloruro de potasio y compárala con la solubilidad del azúcar y de la sal.
Diles a los alumnos que trazarán la solubilidad del cloruro de potasio en un gráfico proporcionado en la hoja de actividades. Explica que el cloruro de potasio se utiliza como sustituto de la sal para las personas que no deben comer sal de mesa (cloruro de sodio).
| Solubilidad del cloruro de potasio Medida en gramos de soluto disueltos en 100 ml de agua | ||||||
| Temperatura °C | 0 | 20 | 40 | 60 | 80 | 100 |
| Cloruro de potasio | 28 | 33 | 38 | 44 | 50 | 55 |
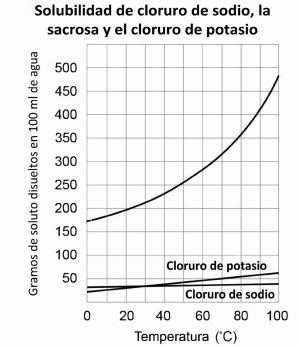
Pregunta a los alumnos:
- ¿A qué temperatura dirías que la solubilidad del cloruro de sodio y del cloruro de potasio es aproximadamente la misma?
- A 0 °C, ¿qué sustancia es la menos soluble?
- A 0 °C, ¿qué sustancia es la más soluble?
¿Qué es el enfoque 5-E?
El modelo de instrucción 5-E es un enfoque de enseñanza y aprendizaje que se centra en la participación activa, el aprendizaje basado en la investigación y la colaboración.
Simulaciones
Vea todas las imágenes de la Lección 5.6 en la página de simulaciónes.
Descargas
Para los estudiantes
- Lección 5.6 Hoja de actividades PDF | DOCX | Google Doc
Para los maestros
- Lección 5.6 Plan de lección PDF | DOCX | Google Doc
- Lección 5.6 Respuestas de la hoja de actividades PDF | DOCX | Google Doc
Recursos para el Capítulo 5
- Capítulo 5 Lectura de estudiantes PDF | DOCX | Google Doc
- Capítulo 5 Banco de pruebas PDF | DOCX | Google Doc
¿Tiene preguntas? Visita el Centro de ayuda