El aire está ahí de verdad
Video de resumen de la leccion para maestros
Nota: Este video está diseñado para ayudar al maestro a comprender mejor la lección y NO está destinado a ser mostrado a los estudiantes. Incluye observaciones y conclusiones que los estudiantes deben hacer por sí solos.
Los subtítulos están disponibles en inglés y español para todos los videos.
Conceptos clave
- En un gas, las partículas (átomos y moléculas) tienen puntos débiles entre sí. Son capaces de moverse libremente entre sí con poca interacción entre ellas.
- Las partículas de un gas están mucho más dispersas y se mueven de forma más independiente en comparación con las partículas de líquidos y sólidos.
- El hecho de que una sustancia sea un sólido, líquido o gas a una temperatura determinada depende del equilibrio entre el movimiento de las partículas a esa temperatura y la intensidad de sus atracciones entre sí.
- El calentamiento de un gas aumenta la velocidad de sus átomos o moléculas.
- El enfriamiento de un gas disminuye la velocidad de sus átomos o moléculas.
Resumen
Los alumnos comparan la masa de una pelota de baloncesto cuando está desinflada y después de inflarse. La pelota inflada tiene la mayor masa, por lo que los alumnos pueden concluir que el gas es materia porque tiene masa y ocupa espacio. A continuación, los alumnos tienen en cuenta cómo afecta el calentamiento y la refrigeración al movimiento molecular en los gases. Sumergen la boca de una botella en una solución de detergente y observan una burbuja que crece y se encoge cuando la botella se calienta y enfría. Los alumnos aprenderán que las atracciones entre las partículas de gases son débiles en comparación con las atracciones entre las partículas de líquidos o sólidos.
Objetivo
Los alumnos podrán describir el gas como materia. También podrán describir, a nivel molecular, el efecto del calentamiento y enfriamiento sobre el movimiento de las moléculas de un gas.

Seguridad
- Asegúrate de que tú y los alumnos usen las gafas protectoras adecuadas.
- Los alumnos deben tener cuidado al manipular agua caliente del grifo.
Materiales para cada grupo
- 2 vasos de plástico transparente
- Botella de plástico de 8 onzas
- Solución de detergente en una taza
- Agua caliente (aproximadamente a 50 °C)
- Agua fría
Materiales para la demostración
- Pelota de baloncesto, muy desinflada
- Balanza que mida en gramos
- Bomba
- Lata de gas comprimido (disponible en cualquier tienda de suministros de oficina)
Descarga todos los recursos de la Lección 1.5
Obtenga el plan de lección completo y la hoja de actividades para la "Lección 1.5: El aire está ahí de verdad."
Instrucciones
1 Involúcrate
Paso 1
Comenta con los alumnos si creen que el gas es materia.
Pregunta a los alumnos sobre los gases:
- Los gases, como los gases en el aire, ¿son materia?
Los alumnos pueden tener preguntas sobre si los gases son materia o no. También pueden tener una sensación muy poco clara de lo que son los gases. Después de que los alumnos respondan, explica que el aire que los rodea está compuesto por algunos gases diferentes: nitrógeno, oxígeno, dióxido de carbono, vapor de agua y cantidades muy pequeñas de algunos otros. Diles a los alumnos que los gases están hechos de moléculas, pero que las moléculas están mucho más separadas que las moléculas en líquidos o sólidos. Dado que las moléculas de un gas tienen masa y ocupan espacio, el gas es materia.
Si los alumnos tienen problemas para aceptar o apreciar que un gas está compuesto por moléculas, podrías intentar ayudarles dándoles algunos números en los que pensar. Aunque estos números son enormes y pueden ser difíciles de comprender, al menos los alumnos tendrán la idea de que un gas está hecho definitivamente de algo, ocupa espacio y tiene masa. Diles a los alumnos que en una cantidad de aire del tamaño de una pelota de playa estándar hay unas 6 × 1023 moléculas de gas. Se trata de unos 600 mil millones de trillones de moléculas.
Los alumnos pueden tener dificultades para imaginar que los gases tienen masa. Parece que los globos y las pelotas de playa, por ejemplo, se vuelven más ligeros cuando los inflamos. Cuando agrega aire a un globo o a una pelota de playa, se hace un poco más pesada. El motivo por el que parece más ligero no es porque tenga menos masa, sino porque su volumen aumenta tanto cuando se infla. Este gran aumento de volumen con un pequeño aumento de masa hace que el globo o la pelota de playa sean menos densos. Por eso parece más ligero cuando se infla. (Podremos llegar a esto cuando estudiemos la densidad en el Capítulo 3).
Paso 2
Haz una demostración para mostrar que el gas tiene masa.
Necesitarás una balanza que mida en gramos para cada demostración. Si no tienes este tipo de balanza, puedes mostrar videos de cada demostración.
Materiales para la demostración
- Pelota de baloncesto, muy desinflada
- Balanza que mida en gramos
- Bomba
- Lata de gas comprimido (disponible en cualquier tienda de suministros de oficina)

Procedimiento
A. Pelota de baloncesto
- Coloca la pelota desinflada en la balanza para obtener la masa inicial.
- Pregunta a los alumnos si creen que la pelota pesará más o menos después de bombear aire hacia ella.

- Bombea todo el aire que puedas en la pelota de baloncesto y vuelve a colocarla en la balanza.

B. Lata de aire comprimido
- Coloca una lata de aire comprimido sobre una balanza y compruebe su masa.
- Pregunta a los alumnos si pesará más, menos o lo mismo si aprietas el gatillo y dejas salir algo de aire.

- Saca el aire de la lata durante unos segundos y luego vuelve a colocar la lata en la alanza.
Resultados esperados
La pelota de baloncesto debe pesar entre 2 y 4 gramos más que cuando se desinfló. La lata pesará unos gramos menos que al principio.
Paso 3
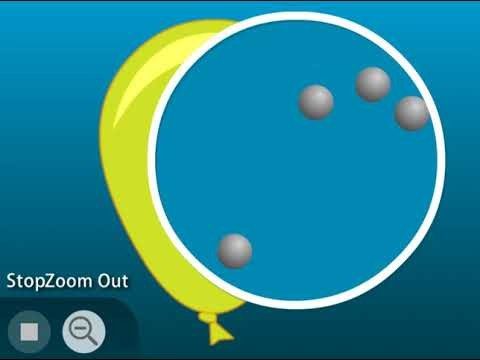
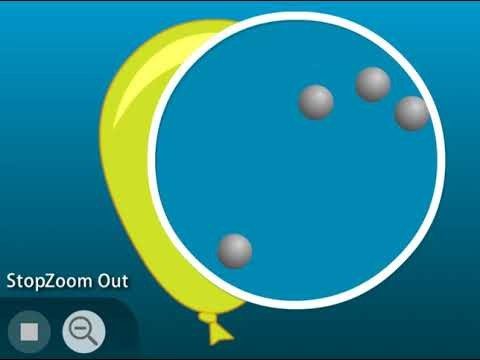
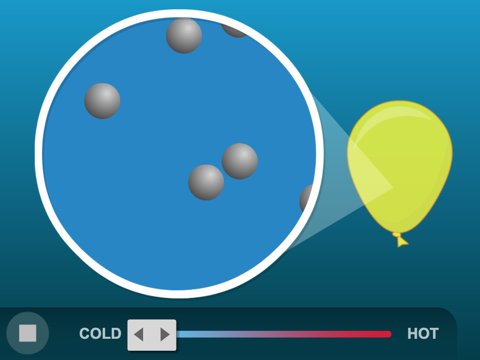
Muestra una animación de las moléculas de un gas.
Muestra la animación del modelo molecular Partículas de un gas.
Explica a los alumnos que las moléculas de un gas tienen muy poca atracción entre sí y que apenas interactúan entre sí. Solo chocan y rebotan. Puede ser difícil de aceptar para los alumnos, pero en el espacio entre las moléculas de gas no hay nada.
Nota: Un alumno curioso podría preguntar: Si las moléculas de gas no se ven atraídas entre sí y pueden flotar, ¿por qué no flotan todas? Esa es una muy buena pregunta. De hecho, los gases muy ligeros como el hidrógeno y el helio han flotado lejos y hay muy pocos gases en nuestra atmósfera. Los gases más pesados y diferentes, como el nitrógeno, el oxígeno, el vapor de agua y el dióxido de carbono, rodean la Tierra. En general, la gravedad mantiene estos gases cerca de la Tierra como nuestra atmósfera.
2 Evalúa
Entrega a cada alumno una hoja de actividades.
- Lección 1.5 Hoja de actividades PDF | DOCX | Google Doc
- Lección 1.5 Respuestas de la hoja de actividades PDF | DOCX | Google Doc
Descarga la hoja de actividades y distribuya una por alumno.
La hoja de actividades servirá como el componente de evaluación de cada plan de lección 5-E. Las hojas de actividades son evaluaciones formativas del progreso y la comprensión de los alumnos. Al final de cada capítulo se incluye una evaluación sumativa más formal.
Los alumnos responderán preguntas sobre la demostración en la hoja de actividades. Las secciones Explícalo con átomos y moléculas y Aprende más de la hoja de actividades se completarán en conjunto con la clase, en grupos o individualmente, según tus instrucciones. Observa la versión para el maestro de la hoja de actividades para encontrar las preguntas y respuestas.
3 Explora
Paso 4
Haz que los alumnos realicen una actividad para averiguar cómo afecta la calefacción y refrigeración a los gases.
Pregunta para investigar
¿Cómo afecta la calefacción y refrigeración a un gas?
Materiales para cada grupo
- 2 vasos de plástico transparente
- Botella de plástico de 8 onzas
- Solución de detergente en una taza
- Agua caliente (aproximadamente a 50 °C)
- Agua fría
Preparación del maestro
Prepara la solución de detergente para toda la clase agregando 4 cucharaditas de líquido lavavajillas y 4 cucharaditas de azúcar a ½ taza de agua. Revuelve suavemente hasta que el detergente y el azúcar se disuelvan. Coloca aproximadamente 1 cucharada de solución de detergente en un vaso ancho de plástico transparente para cada grupo.

Procedimiento
A. Calentar el aire dentro de la botella
- Vierte agua caliente en un vaso vacío hasta que esté aproximadamente ½ lleno.
- Gira la botella y sumerge la abertura de la botella en el detergente para obtener una película de detergente que cubra el borde.

- Mientras sostienes la botella, empuja lentamente el fondo hacia abajo en el agua caliente.
Pregunta a los alumnos:
- ¿Qué puedes hacer para que la burbuja baje?
Si los alumnos tienen problemas para pensar en una respuesta, recuérdales que calentar el gas aumentó la velocidad de las moléculas, lo que hizo que la burbuja creciera. Los alumnos deben sugerir que se enfríe el gas de la botella. Esto se puede hacer colocando la base de la botella en agua fría.

B. Enfriar el aire dentro de la botella
- Vierte agua fría en otra taza hasta que esté llena casi a la mitad.
- Si todavía hay burbujas en la botella, empuja lentamente el fondo hacia abajo en el agua fría.
- Si aún no hay burbujas en la botella, haz otra burbuja sumergiendo la abertura en detergente y luego empujando el fondo de la botella hacia el agua caliente de nuevo.
- Mientras sostienes la botella, empuja lentamente el fondo hacia abajo en el agua fría.
Resultados esperados
Cuando la botella se coloca en agua caliente, se forma una burbuja en la parte superior de la botella. Cuando la botella se coloca en agua fría, la burbuja se hace más pequeña. Es posible que se empuje hacia abajo en la botella.
Paso 5
Registra y comenta las observaciones de los alumnos.
Después de la actividad, da tiempo a los alumnos para que registren sus observaciones respondiendo a las siguientes preguntas en la hoja de actividades. Una vez que hayan respondido las preguntas, comenta sus observaciones en grupo.
- ¿Qué pasó con la película de solución de detergente cuando colocaste la botella en agua caliente?
Se formó una burbuja.
- ¿Qué le pasó a la burbuja cuando colocaste la botella en agua fría?
Se encogió y entró en la botella.
Diles a los alumnos que les mostrarás una animación para ayudar a explicar qué hizo que la burbuja creciera y se encogiera cuando el aire de la botella se calentó y enfrió.
4 Explica
Paso 6
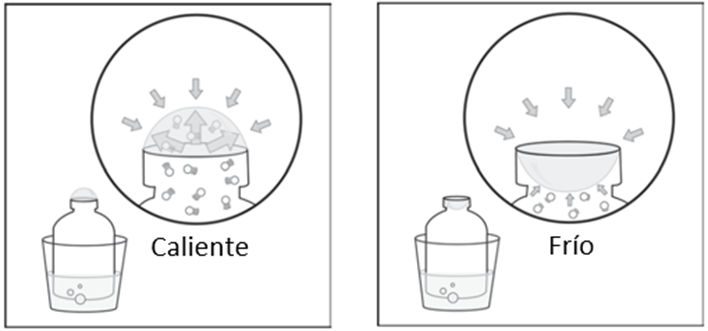
Muestra una animación de una burbuja a medida que se calienta y enfría.
Muestra la animación Calentar y enfriar un gas en una botella.
Diles a los alumnos que las flechas rojas de la animación representan el aire exterior que empuja hacia abajo la película de burbujas. Explica que calentar el aire dentro de la botella hace que las moléculas se muevan más rápido. Estas moléculas de movimiento más rápido golpean el interior de la botella y la película de burbujas más fuerte y con mayor frecuencia. Estas moléculas presionan contra el interior de la película de burbujas más fuerte que el aire circundante empuja desde el exterior. Esto empuja la película de burbuja hacia arriba y hacia fuera, formando una burbuja.
El enfriamiento del gas hace que las moléculas se muevan más lentamente. Estas moléculas de movimiento más lento golpean el interior de la botella y la película de burbujas con menos frecuencia y menos fuerza. Las moléculas del aire circundante se mueven más rápido y empujan contra la burbuja desde el exterior. Dado que estas moléculas externas son más fuertes, la burbuja se empuja hacia abajo y se hace más pequeña.
Paso 7
Pide a los alumnos que respondan las preguntas sobre el crecimiento y la contracción de la burbuja en la hoja de actividades.
Concede a los estudiantes tiempo para responder las siguientes preguntas. Deben consultar el dibujo incluido en la página siguiente y en la hoja de actividades.
Una vez que hayan respondido las preguntas, comenta sus explicaciones en grupo.
- ¿Qué hizo que se formara la burbuja cuando colocaste la botella en agua caliente? Asegúrate de escribir sobre la velocidad de las moléculas dentro de la botella y la presión del aire exterior.
Señala que las moléculas de aire dentro de la botella se mueven más rápido cuando se calientan y empujan más fuerte contra el aire exterior. Esto hace que se forme una burbuja. - ¿Por qué se redujo el tamaño de la burbuja al colocar la botella en agua fría? Asegúrate de escribir sobre la velocidad de las moléculas dentro de la botella y la presión del aire exterior.
Cuando se enfría el aire dentro de la botella, las moléculas se mueven más lentamente y no empujan con tanta fuerza contra el aire exterior. El aire exterior empuja contra la burbuja, haciendo que baje.
Lee más sobre la contracción y expansión de los gases en la sección Información contextual para el maestro.
- Información contextual para el maestro PDF
Paso 8
Haz que los alumnos comparen las moléculas en sólidos, líquidos y gases.
Muestra la animación del modelo molecular Comparar sólidos, líquidos y gases.
Asegúrate de que los alumnos se den cuenta de que las moléculas mostradas provienen de tres sustancias diferentes, todas a temperatura ambiente. El sólido no se derrite para convertirse en un líquido y el líquido no se evapora para convertirse en un gas. El modelo no está intentando mostrar los cambios de estado, sino tres sustancias diferentes (como metal, agua y aire), que son sólidos, líquidos y gases a temperatura ambiente.
Explica las siguientes diferencias a los alumnos:
- Sólido: las partículas (átomos o moléculas) se atraen mucho entre sí. Vibran, pero no se desplazan unas por encima de otras. Los átomos o moléculas permanecen en posiciones fijas debido a su fuerte atracción entre sí. Un sólido tiene un volumen definido y una forma definida.
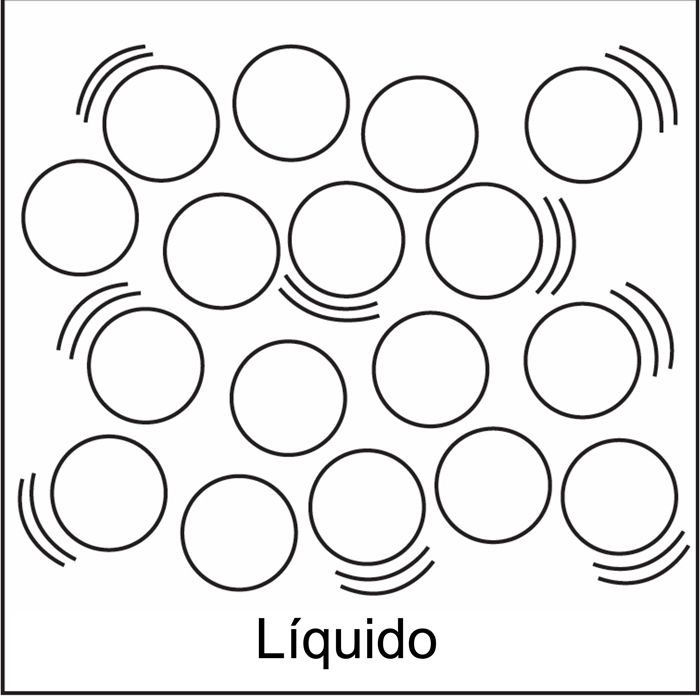
- Líquido: las partículas (átomos o moléculas) se atraen entre sí. Vibran, pero también son capaces de desplazarse unas por encima de otras. Un líquido tiene un volumen definido, pero no tiene una forma definida.
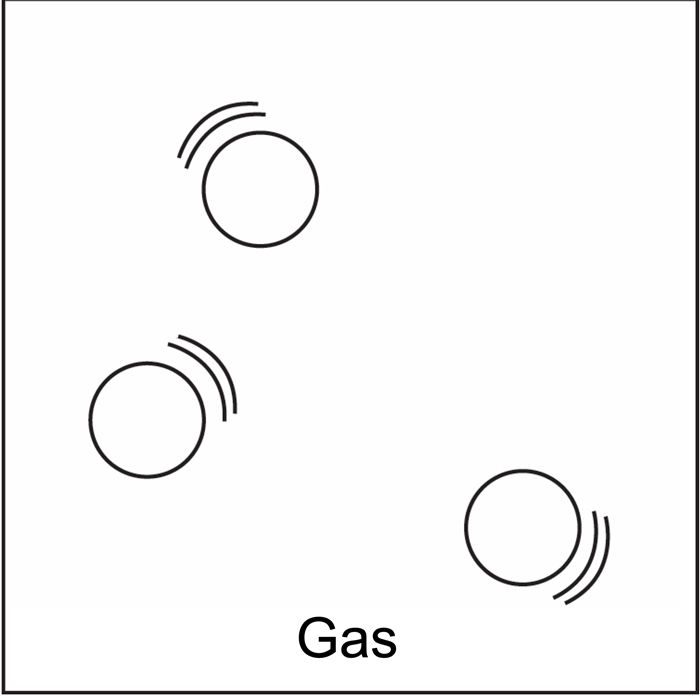
- Gas: las partículas (átomos o moléculas) no se atraen mucho entre sí y se mueven libremente. Un gas no tiene una forma o volumen definidos. Los átomos o moléculas de un gas se esparcen uniformemente para llenar cualquier recipiente.
Puedes utilizar el siguiente ejemplo para ayudar a los alumnos a apreciar la separación entre las moléculas de un gas y las moléculas de un líquido o un sólido:
- Las moléculas que componen un gas están aproximadamente entre 100 y 1000 veces más separadas que las moléculas de un sólido o líquido. Imagina cómo es una cucharada de agua. Si ese mismo número de moléculas fuera un gas, se extenderían lo suficiente como para llenar toda una pelota de playa. A temperatura ambiente, se mueven a unas 1000 millas por hora, pero en distancias muy cortas.
Dibuja o proyecta la ilustración Sólido, líquido y gas.
Haz que los alumnos utilicen la ilustración proyectada como referencia mientras dibujan un modelo de sólidos, líquidos y gases en su hoja de actividades. Señala que el número de líneas de movimiento es el mismo para el sólido, el líquido y el gas. Esto indica que las diferentes sustancias están a la misma temperatura. Haz que los alumnos escriban subtítulos como los que se enumeran a continuación para describir las moléculas en sólidos, líquidos y gases
5 Amplía
Paso 9
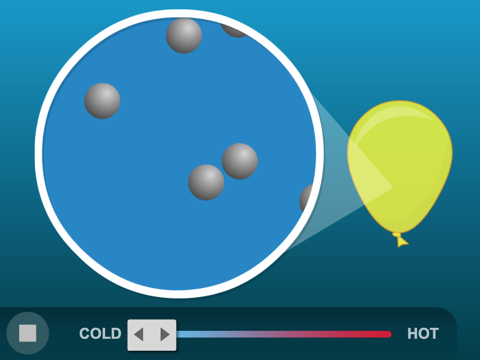
Haz que los alumnos apliquen lo que han aprendido para explicar por qué un globo crece cuando se calienta.
Pide a los alumnos que consideren la siguiente situación:
Imagina que trabajas en una tienda de fiestas durante el verano. Vas a conducir a casa con el propietario de la tienda cuyo coche ha estado bajo el sol durante todo el día. El propietario te dice que puedes llevarte a casa una enorme cantidad de globos, pero te aconseja que no infles los globos por completo. Sabiendo lo que sabes acerca de calentar las moléculas de un gas, explica por qué el consejo del propietario es inteligente.
Puedes optar por mostrar la animación Calentar moléculas de un gas si deseas dar una pista a los estudiantes.
¿Qué es el enfoque 5-E?
El modelo de instrucción 5-E es un enfoque de enseñanza y aprendizaje que se centra en la participación activa, el aprendizaje basado en la investigación y la colaboración.
Simulaciones
Descargas
Para los estudiantes
- Lección 1.5 Hoja de actividades PDF | DOCX | Google Doc
Para los maestros
- Lección 1.5 Plan de lección PDF | DOCX | Google Doc
- Lección 1.5 Respuestas de la hoja de actividades PDF | DOCX | Google Doc
- Lección 1.5 Información contextual para el maestro PDF
Recursos para el Capítulo 1
- Capítulo 1 Lectura de estudiantes PDF | DOCX | Google Doc
- Capítulo 1 Banco de pruebas PDF | DOCX | Google Doc
¿Tiene preguntas? Visita el Centro de ayuda