Lección 4.5: Niveles de energía, electrones y enlaces iónicos
Lección de acompañamiento: Lección 4.5: Niveles de energía, electrones y enlaces iónicos
Video
El sodio y el cloro reaccionan
- Se coloca un pequeño trozo de metal de sodio en un matraz con gas de cloro.
- Un poco de agua ayuda a exponer el sodio para que pueda reaccionar con el gas de cloro.
- La reacción libera mucho calor a medida que se forma el compuesto iónico cloruro de sodio.
La demostración que se muestra en este video es muy peligrosa. No intentes realizar esta demostración.
Este video aparece como cortesía de Chemical Education Exchange (ChemEd X)
Interactivo
Enlace iónico en cloruro de sodio 1
- Un átomo de sodio y un átomo de cloro están cerca el uno del otro.
- Un electrón de cada átomo siente la atracción del núcleo del otro átomo.
- La atracción que ejerce el cloro es más fuerte que la que ejerce el sodio.
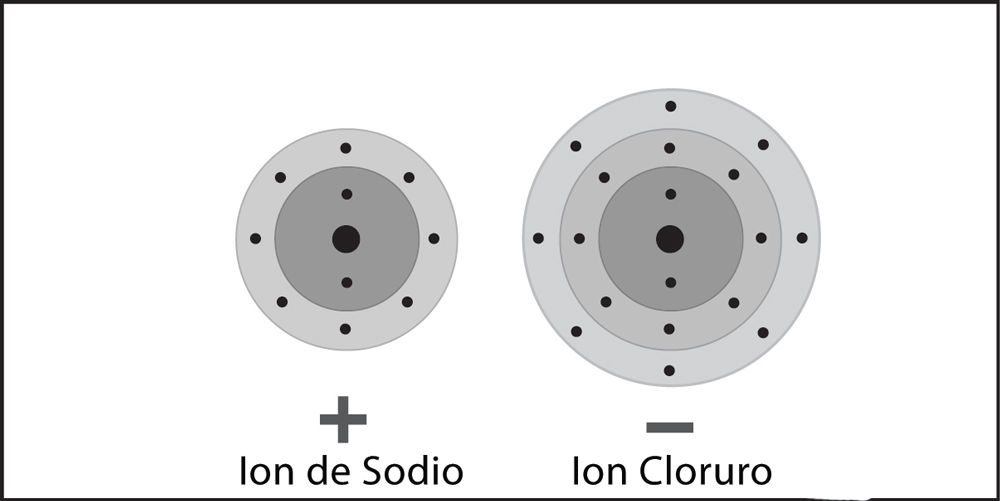
- Se transfiere un electrón del sodio al cloro. El sodio se convierte en un ion positivo y el cloro se convierte en un ion negativo.
- Los iones positivos y negativos se atraen entre sí y forman el compuesto iónico cloruro de sodio.
Imagen
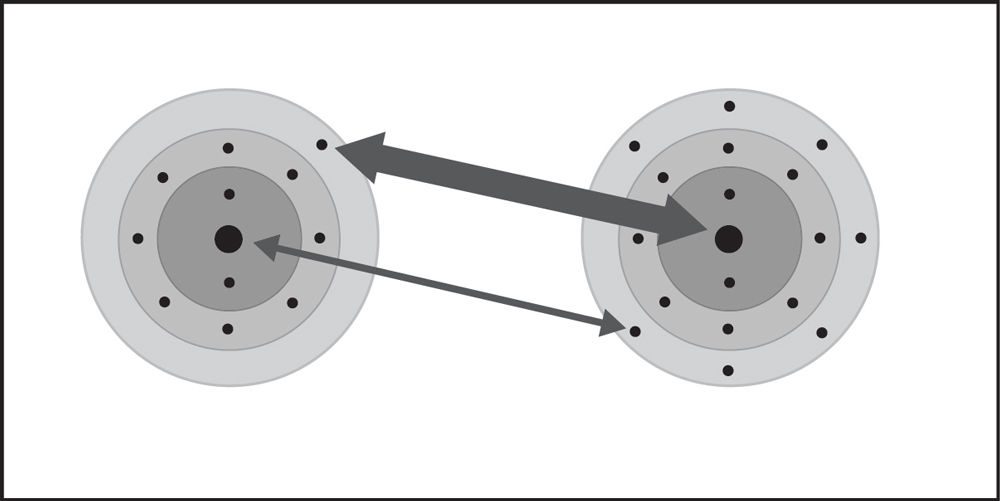
Enlace iónico en cloruro de sodio 2
- Un átomo de sodio y un átomo de cloro están cerca el uno del otro.
- Un electrón de cada átomo siente la atracción del núcleo del otro átomo.
- La atracción que ejerce el cloro es más fuerte que la que ejerce el sodio.
- Se transfiere un electrón del sodio al cloro. El sodio se convierte en un ion positivo y el cloro se convierte en un ion negativo.
- Los iones positivos y negativos se atraen entre sí y forman el compuesto iónico cloruro de sodio.
Video
Cristal de cloruro de sodio
- El cristal de cloruro de sodio está formado por iones de sodio y cloruro alternados.
Este video aparece como cortesía de Roy Tasker, VisChem Project
Imagen
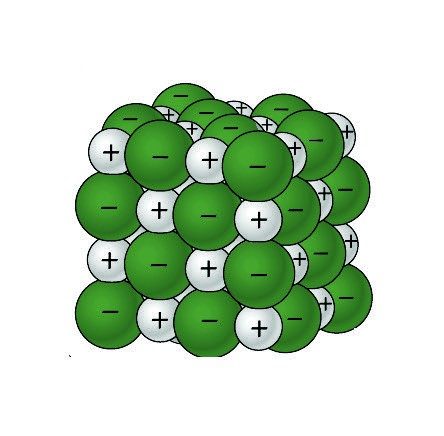
Cloruro de sodio cúbico
- Cuando se examinan de cerca los cristales de sal bajo un microscopio, puede verse su forma cúbica.
Interactivo
Enlace iónico de cloruro de calcio 1
- Un átomo de calcio y dos átomos de cloro están cerca entre sí.
- Un electrón de cada átomo siente la atracción del núcleo del otro átomo.
- La atracción que ejercen los átomos de cloro es más fuerte que la que ejerce el átomo de calcio.
- Se transfieren dos electrones del átomo de calcio, uno a cada átomo de cloro.
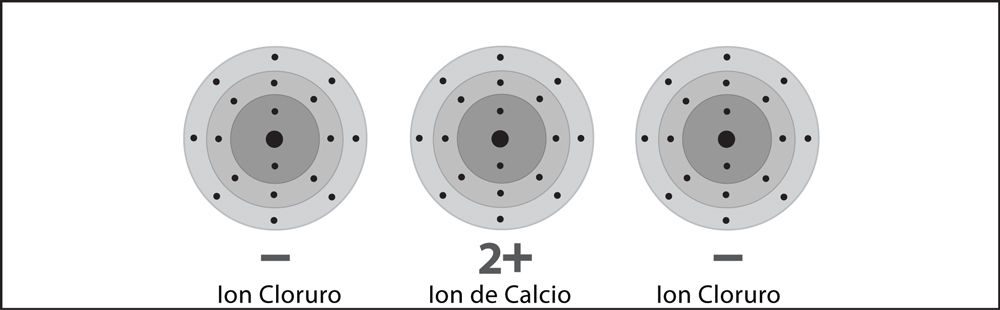
- El calcio se convierte en un ion +2 y cada cloruro se convierte en un ion -1. El ion de calcio +2 y los dos iones cloruro -1 se atraen entre sí, formando un enlace iónico y el compuesto cloruro de calcio.
Imagen
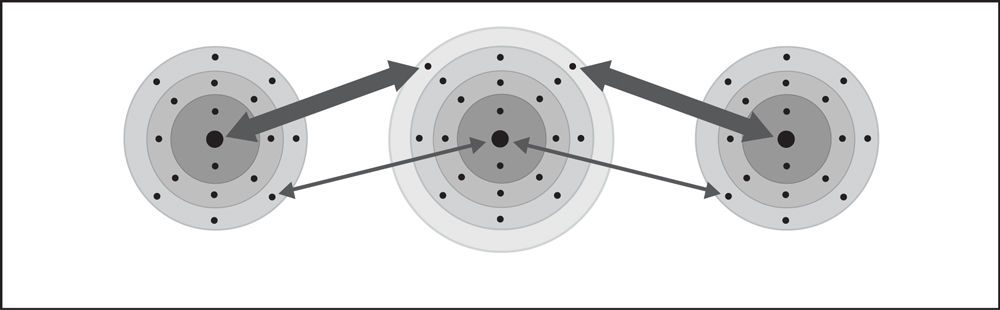
Enlace iónico de cloruro de calcio 2
- Un átomo de calcio y dos átomos de cloro están cerca entre sí.
- Un electrón de cada átomo siente la atracción del núcleo del otro átomo.
- La atracción que ejercen los átomos de cloro es más fuerte que la que ejerce el átomo de calcio.
- Se transfieren dos electrones del átomo de calcio, uno a cada átomo de cloro.
- El calcio se convierte en un ion +2 y cada cloruro se convierte en un ion -1. El ion de calcio +2 y los dos iones cloruro -1 se atraen entre sí, formando un enlace iónico y el compuesto cloruro de calcio.