Lección 5.1: El agua es una molécula polar
Lección de acompañamiento: Lección 5.1: El agua es una molécula polar
Video
Globo de agua
- Las moléculas de agua se atraen tanto entre sí que, incluso después de que el globo explota, las moléculas se mantienen unidas y el globo conserva su forma.
Video
Fuente de agua
- El agua permanece unida porque las moléculas de agua se atraen entre sí.
Interactivo
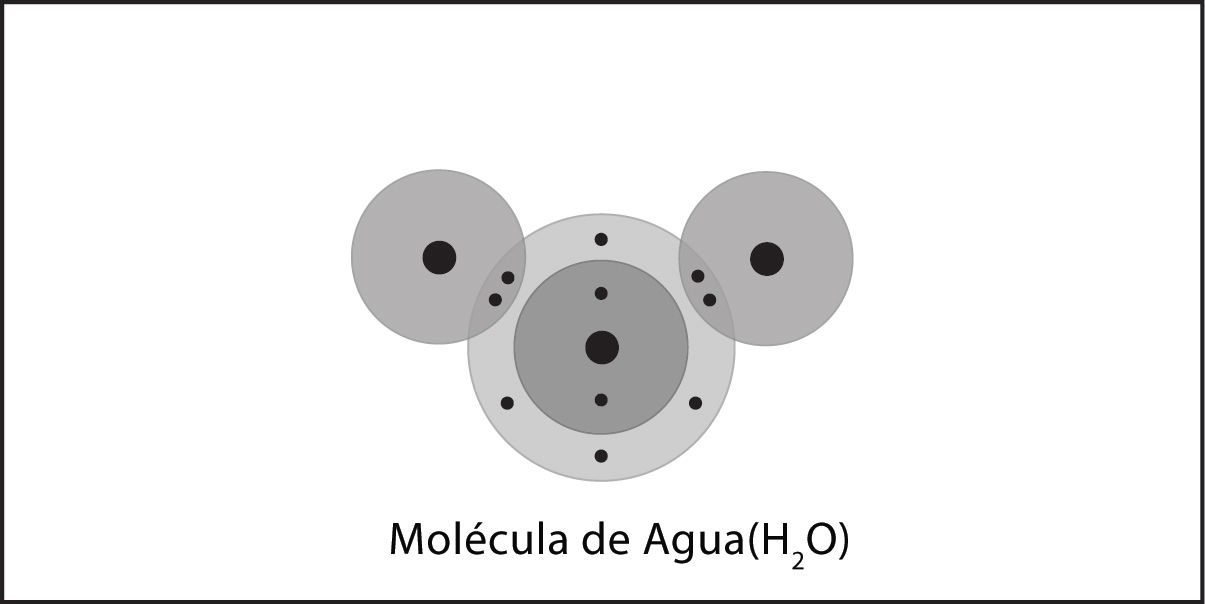
Molécula de agua polar
- En la molécula de agua, los átomos de oxígeno e hidrógeno comparten electrones en enlaces covalentes.
- Hay un total de 10 protones y 10 electrones, por lo que la molécula de agua es neutra.
- El modelo de la nube de electrones muestra que los electrones no se comparten por igual en la molécula de agua.
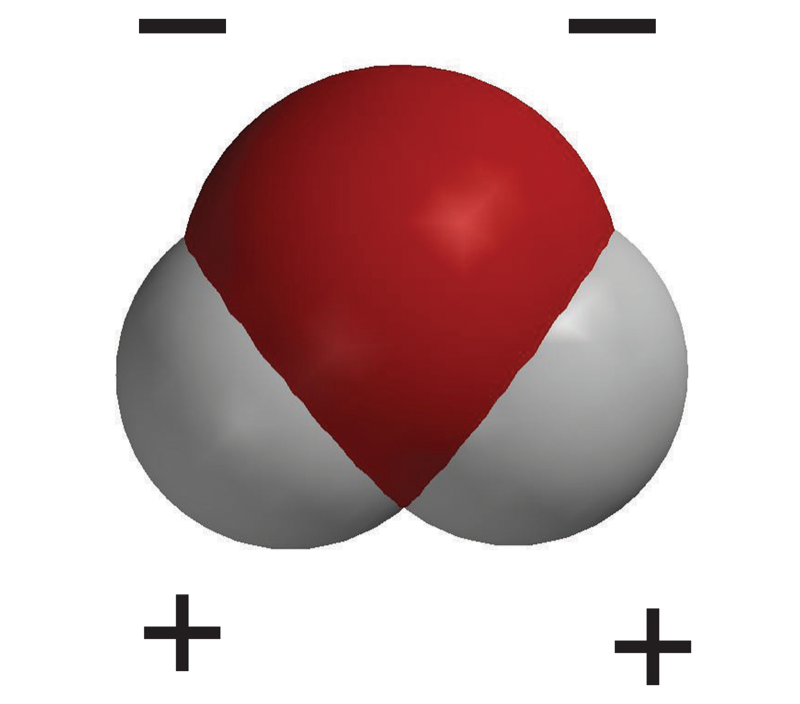
- Los electrones sienten un poco más de atracción por el átomo de oxígeno que por los átomos de hidrógeno.
- Esto hace que la molécula de agua sea ligeramente negativa en el extremo del oxígeno y ligeramente positiva en el extremo del hidrógeno.
Video
Atracción entre moléculas de agua
- Las moléculas de agua tienden a orientarse con el área positiva de una molécula cerca del área negativa de otra.
Imagen
Atracciones a diferentes niveles
- Los electrones se ven atraídos por los protones dentro de un átomo. Esto es lo que mantiene unido el átomo.
- Los electrones se ven atraídos por los protones de otros átomos. Esto es lo que hace que los átomos se unan y lo que mantiene unida una molécula.
- Los electrones se pueden compartir de forma desigual en una molécula, creando una molécula polar. Los extremos polares opuestos de las moléculas atraen y fijan una molécula a la otra.